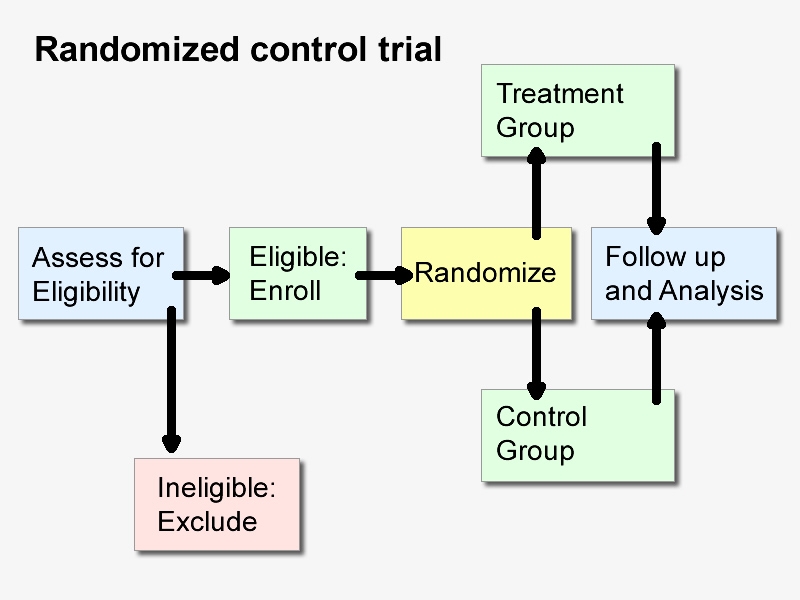
Les essais contrôlés randomisés (ECR) constituent la référence absolue pour évaluer l'innocuité et l'efficacité d'un traitement. Cependant, dans certains cas, les ECR ne sont pas réalisables. C'est pourquoi certains chercheurs proposent de concevoir des études observationnelles selon le principe de l'ECR, c'est-à-dire de simuler des études observationnelles en ECR afin d'en améliorer la validité.
Les essais contrôlés randomisés (ECR) sont des critères permettant d'évaluer la sécurité et l'efficacité relatives des interventions médicales. Bien que les analyses de données observationnelles issues d'études épidémiologiques et de bases de données médicales (notamment les dossiers médicaux électroniques [DME] et les données relatives aux demandes de remboursement) présentent l'avantage de disposer d'échantillons importants, d'un accès rapide aux données et de la possibilité d'évaluer les effets en situation réelle, ces analyses sont sujettes à des biais qui affaiblissent la solidité des preuves qu'elles produisent. Il est depuis longtemps suggéré de concevoir des études observationnelles selon les principes des ECR afin d'améliorer la validité des résultats. Plusieurs approches méthodologiques tentent de tirer des conclusions causales à partir de données observationnelles, et un nombre croissant de chercheurs simulent la conception d'études observationnelles sur des ECR hypothétiques par le biais de la « simulation d'essais ciblés ».
Le cadre de simulation d'essais cibles exige que la conception et l'analyse des études observationnelles soient cohérentes avec celles des ECR hypothétiques portant sur la même question de recherche. Bien que cette approche structurée de conception, d'analyse et de reporting puisse améliorer la qualité des études observationnelles, les études menées de cette manière restent sujettes à des biais provenant de sources multiples, notamment des effets de confusion liés à des covariables non observées. De telles études nécessitent des éléments de conception détaillés, des méthodes analytiques pour traiter les facteurs de confusion et des rapports d'analyse de sensibilité.
Dans les études utilisant la méthode de simulation d'essais ciblés, les chercheurs établissent un essai clinique randomisé (ECR) hypothétique, idéalement réalisé pour résoudre un problème de recherche particulier, puis définissent les éléments de conception de l'étude observationnelle compatibles avec cet ECR « test cible ». Ces éléments de conception comprennent l'inclusion de critères d'exclusion, la sélection des participants, la stratégie thérapeutique, l'attribution des traitements, le début et la fin du suivi, les mesures de résultats, l'évaluation de l'efficacité et le plan d'analyse statistique (PAS). Par exemple, Dickerman et al. ont utilisé un cadre de simulation d'essais ciblés et appliqué les données du DSE du Département des anciens combattants des États-Unis (VA) pour comparer l'efficacité des vaccins BNT162b2 et ARNm-1273 dans la prévention des infections, des hospitalisations et des décès liés au SARS-CoV-2.
Un élément clé de la simulation d'un essai cible est de définir le « temps zéro », le moment où l'éligibilité des participants est évaluée, le traitement est attribué et le suivi est initié. Dans l'étude du VA sur le vaccin contre la Covid-19, le temps zéro a été défini comme la date de la première dose de vaccin. Unifier le moment de la détermination de l'éligibilité, de l'attribution du traitement et du début du suivi au temps zéro réduit d'importantes sources de biais, notamment le biais de temps immortel dans la détermination des stratégies thérapeutiques après le début du suivi, et le biais de sélection lors du début du suivi après l'attribution du traitement. Au VA
Dans l'étude sur le vaccin contre la Covid-19, si les participants étaient assignés au groupe de traitement pour l'analyse en fonction du moment où ils avaient reçu la deuxième dose de vaccin, et que le suivi était commencé au moment de la première dose de vaccin, il y avait un biais de non-décès ; si le groupe de traitement est assigné au moment de la première dose de vaccin et que le suivi commence au moment de la deuxième dose de vaccin, un biais de sélection apparaît car seuls ceux qui ont reçu deux doses de vaccin seront inclus.
Les simulations d'essais ciblés permettent également d'éviter les situations où les effets thérapeutiques ne sont pas clairement définis, une difficulté fréquente dans les études observationnelles. Dans l'étude du VA sur le vaccin contre la Covid-19, les chercheurs ont apparié les participants selon leurs caractéristiques initiales et évalué l'efficacité du traitement en fonction des différences de risque à 24 semaines. Cette approche définit explicitement les estimations d'efficacité comme les différences de résultats de la Covid-19 entre des populations vaccinées présentant des caractéristiques initiales équilibrées, à l'instar des estimations d'efficacité des ECR pour le même problème. Comme le soulignent les auteurs de l'étude, la comparaison des résultats de deux vaccins similaires peut être moins influencée par des facteurs de confusion que la comparaison des résultats de personnes vaccinées et non vaccinées.
Même si les éléments sont correctement alignés avec les ECR, la validité d'une étude utilisant un cadre de simulation d'essai cible dépend du choix des hypothèses, de la conception et des méthodes d'analyse, ainsi que de la qualité des données sous-jacentes. Bien que la validité des résultats des ECR dépende également de la qualité de la conception et de l'analyse, les résultats des études observationnelles sont également menacés par des facteurs de confusion. En tant qu'études non randomisées, les études observationnelles ne sont pas à l'abri de facteurs de confusion comme les ECR, et les participants et les cliniciens ne sont pas en aveugle, ce qui peut affecter l'évaluation des résultats et les résultats de l'étude. Dans l'étude du VA sur le vaccin contre la Covid-19, les chercheurs ont utilisé une approche d'appariement pour équilibrer la distribution des caractéristiques initiales des deux groupes de participants, notamment l'âge, le sexe, l'origine ethnique et le degré d'urbanisation du lieu de résidence. Les différences dans la distribution d'autres caractéristiques, telles que la profession, peuvent également être associées au risque d'infection par la Covid-19 et constitueront des facteurs de confusion résiduels.
De nombreuses études utilisant des méthodes de simulation d'essais ciblés utilisent des données du monde réel (DMR), telles que les données du DMP. Les DMR présentent l'avantage d'être rapides, évolutives et représentatives des schémas thérapeutiques conventionnels. Cependant, elles doivent être mises en balance avec les problèmes de qualité des données, notamment les données manquantes, l'identification et la définition inexactes et incohérentes des caractéristiques et des résultats des participants, l'administration inégale des traitements, la fréquence variable des évaluations de suivi et la perte d'accès due au transfert des participants entre différents systèmes de santé. L'étude du VA a utilisé les données d'un DMP unique, ce qui a atténué nos inquiétudes quant aux incohérences des données. Cependant, la confirmation et la documentation incomplètes des indicateurs, notamment des comorbidités et des résultats, demeurent un risque.
La sélection des participants dans les échantillons analytiques repose souvent sur des données rétrospectives, ce qui peut entraîner un biais de sélection en excluant les personnes pour lesquelles les informations initiales sont manquantes. Bien que ces problèmes ne soient pas spécifiques aux études observationnelles, ils constituent des sources de biais résiduels que les simulations d'essais ciblés ne peuvent pas directement traiter. De plus, les études observationnelles ne sont souvent pas préenregistrées, ce qui exacerbe des problèmes tels que la sensibilité du plan d'étude et le biais de publication. Étant donné que des sources de données, des plans d'étude et des méthodes d'analyse différents peuvent produire des résultats très différents, le plan d'étude, la méthode d'analyse et le critère de sélection des sources de données doivent être prédéterminés.
Il existe des directives pour la conduite et la communication d'études utilisant le cadre de simulation d'essais ciblés. Ces directives améliorent la qualité de l'étude et garantissent que le rapport est suffisamment détaillé pour permettre au lecteur de l'évaluer de manière critique. Premièrement, les protocoles de recherche et le SAP doivent être préparés avant l'analyse des données. Le SAP doit inclure des méthodes statistiques détaillées pour traiter les biais dus aux facteurs de confusion, ainsi que des analyses de sensibilité pour évaluer la robustesse des résultats face aux principales sources de biais, telles que les facteurs de confusion et les données manquantes.
Les sections « Titre », « Résumé » et « Méthodes » doivent préciser clairement qu'il s'agit d'une étude observationnelle afin d'éviter toute confusion avec un essai contrôlé randomisé (ECR). Elles doivent également distinguer les études observationnelles déjà réalisées des essais hypothétiques simulés. Le chercheur doit préciser les critères de qualité, tels que la source des données, leur fiabilité et leur validité, et, si possible, citer d'autres études publiées utilisant cette source. L'investigateur doit également fournir un tableau présentant les éléments de conception de l'essai cible et de sa simulation observationnelle, ainsi qu'une indication claire du moment où déterminer l'éligibilité, initier le suivi et prescrire le traitement.
Dans les études utilisant des simulations d'essais ciblés, lorsqu'une stratégie thérapeutique ne peut être déterminée au départ (comme les études sur la durée du traitement ou l'utilisation de thérapies combinées), une résolution du biais non lié au décès doit être décrite. Les chercheurs doivent présenter des analyses de sensibilité significatives afin d'évaluer la robustesse des résultats de l'étude face aux principales sources de biais, notamment en quantifiant l'impact potentiel des facteurs de confusion discrets et en explorant l'évolution des résultats lorsque les éléments clés de la conception sont définis autrement. L'utilisation de résultats de contrôle négatifs (résultats fortement indépendants de l'exposition préoccupante) peut également contribuer à quantifier le biais résiduel.
Bien que les études observationnelles puissent analyser des problèmes qui ne pourraient pas être réalisés dans le cadre d'ECR et tirer parti des données de référence, elles présentent également de nombreuses sources potentielles de biais. Le cadre de simulation d'essais cibles vise à corriger certains de ces biais, mais doit être simulé et rapporté avec soin. Étant donné que les facteurs de confusion peuvent entraîner des biais, des analyses de sensibilité doivent être réalisées pour évaluer la robustesse des résultats par rapport aux facteurs de confusion non observés, et les résultats doivent être interprétés de manière à prendre en compte les variations des résultats lorsque d'autres hypothèses sont formulées concernant ces facteurs. Le cadre de simulation d'essais cibles, s'il est rigoureusement mis en œuvre, peut être une méthode utile pour définir systématiquement des plans d'études observationnelles, mais il ne constitue pas une solution miracle.
Date de publication : 30 novembre 2024