L'hyperlipidémie mixte est caractérisée par des taux plasmatiques élevés de lipoprotéines de basse densité (LDL) et de lipoprotéines riches en triglycérides, entraînant un risque accru de maladie cardiovasculaire athéroscléreuse dans cette population de patients.
L'ANGPTL3 inhibe la lipoprotéine lipase et l'endosépiase, ainsi que l'absorption hépatique des lipoprotéines riches en triglycérides. Les porteurs de la variante inactivée de l'ANGPTL3 présentaient des taux plus faibles de triglycérides, de cholestérol LDL, de cholestérol HDL et de cholestérol non HDL, ainsi qu'un risque plus faible de maladie cardiovasculaire athéroscléreuse. Le zodasiran est un petit ARN interférent (ARNi) qui cible l'expression de l'ANGPTL3 dans le foie.
L'hyperlipidémie mixte se caractérise par des taux élevés de cholestérol à lipoprotéines de basse densité (LDL-C) et de lipoprotéines riches en triglycérides. Ces lipoprotéines (dont les chylomicrons, les lipoprotéines de très basse densité (VLDL) et le cholestérol résiduel) jouent un rôle important dans le développement de l'athérosclérose. Il n'existe aucun traitement efficace contre l'hyperlipidémie mixte.
Les Bates sont connus pour réduire le taux de triglycérides (TG), mais cette réduction est limitée. Parallèlement, les médicaments hypoglycémiants, dont les Bates (comme l'acide acétique eicosapentaénoïque, etc.), n'ont pas d'effet significatif sur le risque de maladie athéroscléreuse due à un taux de cholestérol résiduel élevé. De plus, des études antérieures menées chez des patients prenant déjà des statines ont montré que l'association de médicaments hypoglycémiants ne réduit pas le risque d'événements cardiovasculaires. Ces facteurs rendent le traitement de l'hyperlipidémie mixte très difficile.
L'ANGPTL3 (protéine de type angiopoïétine 3) régule le métabolisme des lipides et des lipoprotéines, notamment des triglycérides et du cholestérol HDL-C, en inhibant de manière réversible la captation hépatique dépendante de la lipoprotéine lipase, de l'endosépiase et du récepteur des lipoprotéines de basse densité (LDL). Il a été constaté que la variante d'inactivation de l'ANGPTL3 entraîne une augmentation de l'activité de la lipoprotéine lipase et de l'endosépiase, ce qui entraîne à son tour de faibles taux plasmatiques de lipoprotéines dans la plupart des cas. Celles-ci comprennent les lipoprotéines riches en triglycérides (chylomicrons, cholestérol résiduel, VLDL, lipoprotéines de moyenne densité [IDL]), les LDL, les lipoprotéines de haute densité (HDL), la lipoprotéine (a) et leurs composants cholestérol. Les personnes hétérozygotes porteuses de cette variante présentent un risque réduit d'environ 40 % de développer une maladie athéroscléreuse, et aucun phénotype clinique indésirable n'a été observé. ANGPTL3 est exprimé dans le foie, et les thérapies de silençage génique ciblant son ARNm, appelées médicaments à petits ARN interférents (siARN), constituent un traitement hybride prometteur contre l'hyperlipidémie.
Le 12 septembre 2024, le New England Journal of Medicine (NEJM) a publié une étude ARCHES 2 confirmant que le zodasiran, un médicament siRNA, réduisait significativement les taux de triglycérides chez les patients atteints d'hyperlipidémie mixte [1]. ARCHES-2 est un essai de phase 2b, en double aveugle, contrôlé par placebo, explorant les doses. Au total, 204 patients atteints d'hyperlipidémie mixte (taux de triglycérides à jeun compris entre 150 et 499 mg/dL, taux de LDL-C supérieur ou égal à 70 mg/dL ou taux de non-HDL-C supérieur ou égal à 100 mg/dL) ont été inclus. Ils ont été répartis en groupes zodasiran 50 mg, 100 mg, 200 mg et un groupe témoin placebo. Les patients ont reçu des injections sous-cutanées aux semaines 1 et 12, et ont bénéficié d'une prophylaxie de suivi jusqu'à la semaine 36.
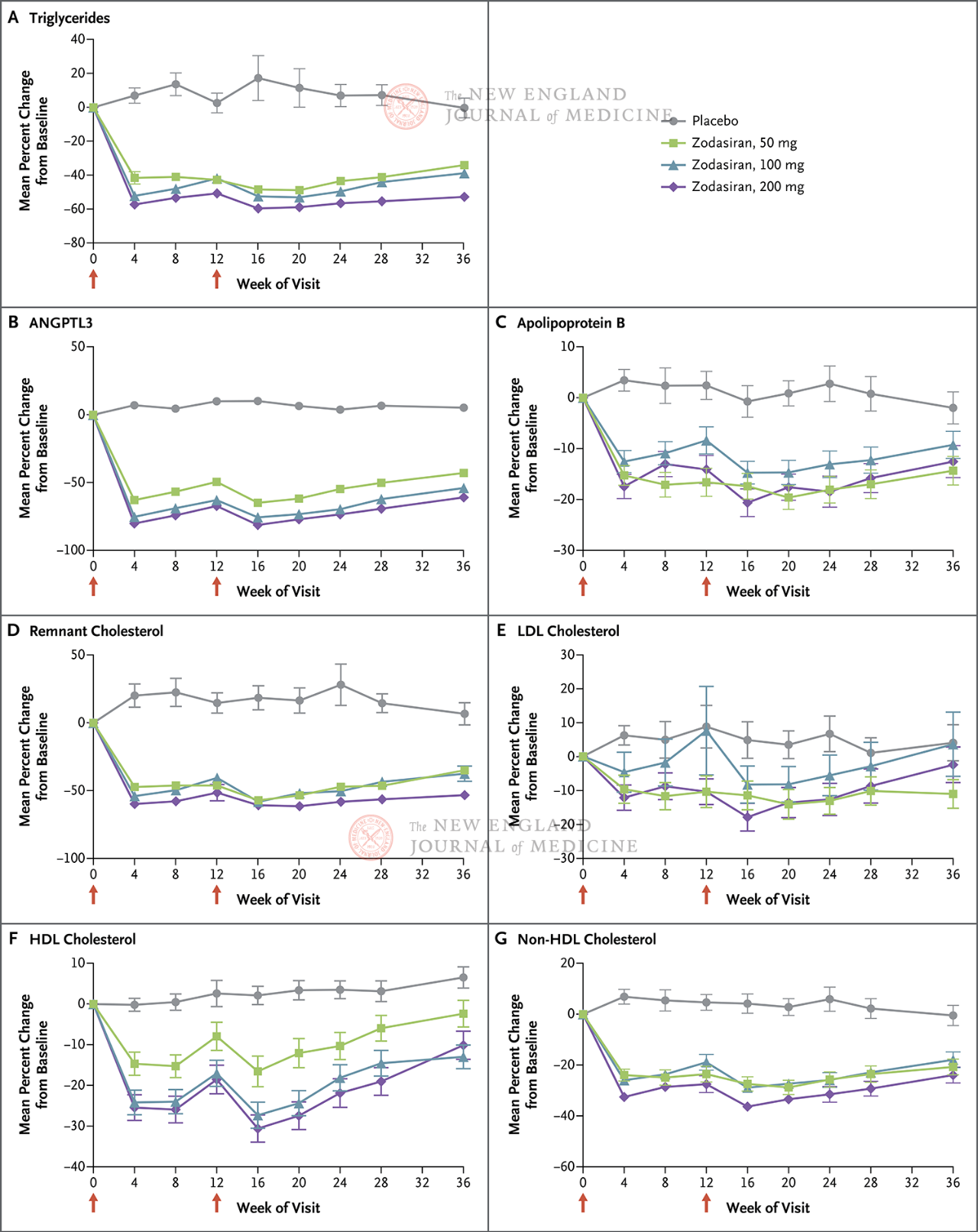
Le critère d'évaluation principal était la variation en pourcentage des TG entre le début de l'étude et la semaine 24. L'étude a révélé qu'à la semaine 24, les taux de TG dans le groupe zodasiran avaient significativement diminué de manière dose-dépendante (les taux de TG dans chaque groupe de dose avaient diminué respectivement de 51, 57 et 63 points de pourcentage par rapport à ceux du groupe placebo) (p < 0,001 pour toutes les comparaisons). L'ANGPTL3 a également diminué respectivement de 54, 70 et 74 points de pourcentage. Les taux de cholestérol non HDL ont diminué respectivement de 29, 29 et 36 points de pourcentage, les taux d'apolipoprotéine B ont diminué respectivement de 19, 15 et 22 points de pourcentage, et les taux de LDL-C ont diminué respectivement de 16, 14 et 20 points de pourcentage. Ces résultats ont persisté jusqu'à la 36e semaine. À la semaine 24, le zodasiran
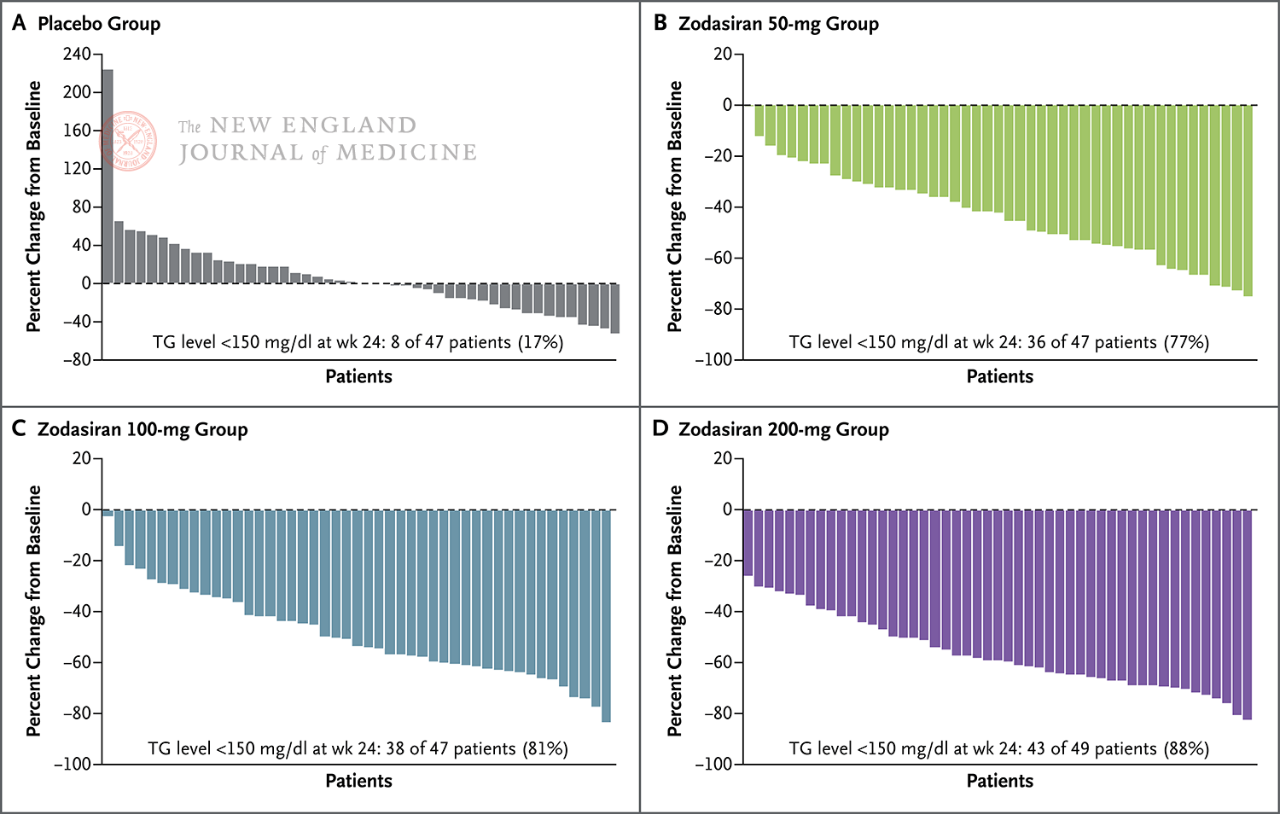
Chez 88 % des patients du groupe 200 mg, la TG à jeun était tombée dans la plage normale.
Les flèches rouges sur les jours 1 et 12 indiquent l’administration de zodasiran ou de placebo.
Les niveaux de TG à jeun sont revenus à la normale à la semaine 24 (150
mg/dL ou moins)
Chaque pilier représente un patient.
Français L'étude a également observé que le zotasiran était sûr dans tous les groupes de dose, avec seulement 2 patients abandonnant l'étude en raison d'événements indésirables (1 dans le groupe placebo et 1 dans le groupe zotasiran 100 mg). Tous les événements indésirables graves dans le groupe zotasiran se sont rétablis à la fin de l'étude, et il y a eu un décès dans le groupe placebo. Le seul événement indésirable préoccupant était une augmentation de l'HBA1c dans le groupe zotasiran 200 mg par rapport au placebo (variation moyenne entre la valeur initiale et la semaine 24 [± ET], 0,38 ± 0,66 % contre -0,03 ± 0,88 % chez les patients atteints de diabète préexistant). Les patients sans diabète étaient de 0,12 ± 0,19 % contre -0,03 ± 0,19 %).
En particulier, la quasi-totalité des patients de l'étude (96 %) étaient traités par statines (dont 37 % à forte dose), 1 % par un inhibiteur de la subtilysine 9 (PCSK9i) et 21 % par fibrates. Par conséquent, l'ajout de zodasiran au schéma thérapeutique conventionnel actuel a permis d'obtenir des effets hypolipémiants significatifs, offrant ainsi un nouveau schéma thérapeutique pour le traitement futur de l'hyperlipidémie mixte.
À la semaine 24, la dose maximale de 200 mg de zotasiran administrée dans l'étude a réduit le taux de cholestérol résiduel de 34,4 mg/dL par rapport au placebo. D'après les modèles actuels, cette réduction devrait réduire de 20 % les événements indésirables cardiaques majeurs. Le zodasiran pourrait être utilisé en monothérapie pour tous les composants lipoprotéiques afin de réduire le risque d'événements cardiovasculaires chez les patients. Des recherches supplémentaires sont donc nécessaires pour déterminer le potentiel de ce médicament à réduire le risque de maladie athéroscléreuse.
L'étude MUIR de phase IIb, randomisée, en double aveugle et contrôlée par placebo, publiée simultanément dans le NEJM, a utilisé un autre médicament siRNA, le plozasiran, pour traiter l'hyperlipidémie mixte [2]. Le plozasiran est conçu pour réduire l'expression d'APOC3, le gène codant pour l'apolipoprotéine C3 (APOC3), un régulateur du métabolisme des triglycérides, dans le foie, réduisant ainsi les taux de triglycérides et de cholestérol résiduel. Les réductions des taux de triglycérides et de cholestérol résiduel observées dans cette étude étaient similaires à celles observées dans l'étude ARCHES-2. Par conséquent, on suppose que chez les patients atteints d'hyperlipidémie mixte, les deux médicaments ont des effets similaires sur la réduction des taux de lipoprotéines riches en triglycérides et de cholestérol résiduel.
Les résultats des deux études siRNA montrent qu’il s’agit d’une classe de médicaments très prometteuse qui apportera de nouvelles options pour le traitement de l’hyperlipidémie mixte et améliorera les résultats cardiovasculaires chez les patients.
Date de publication : 15 septembre 2024