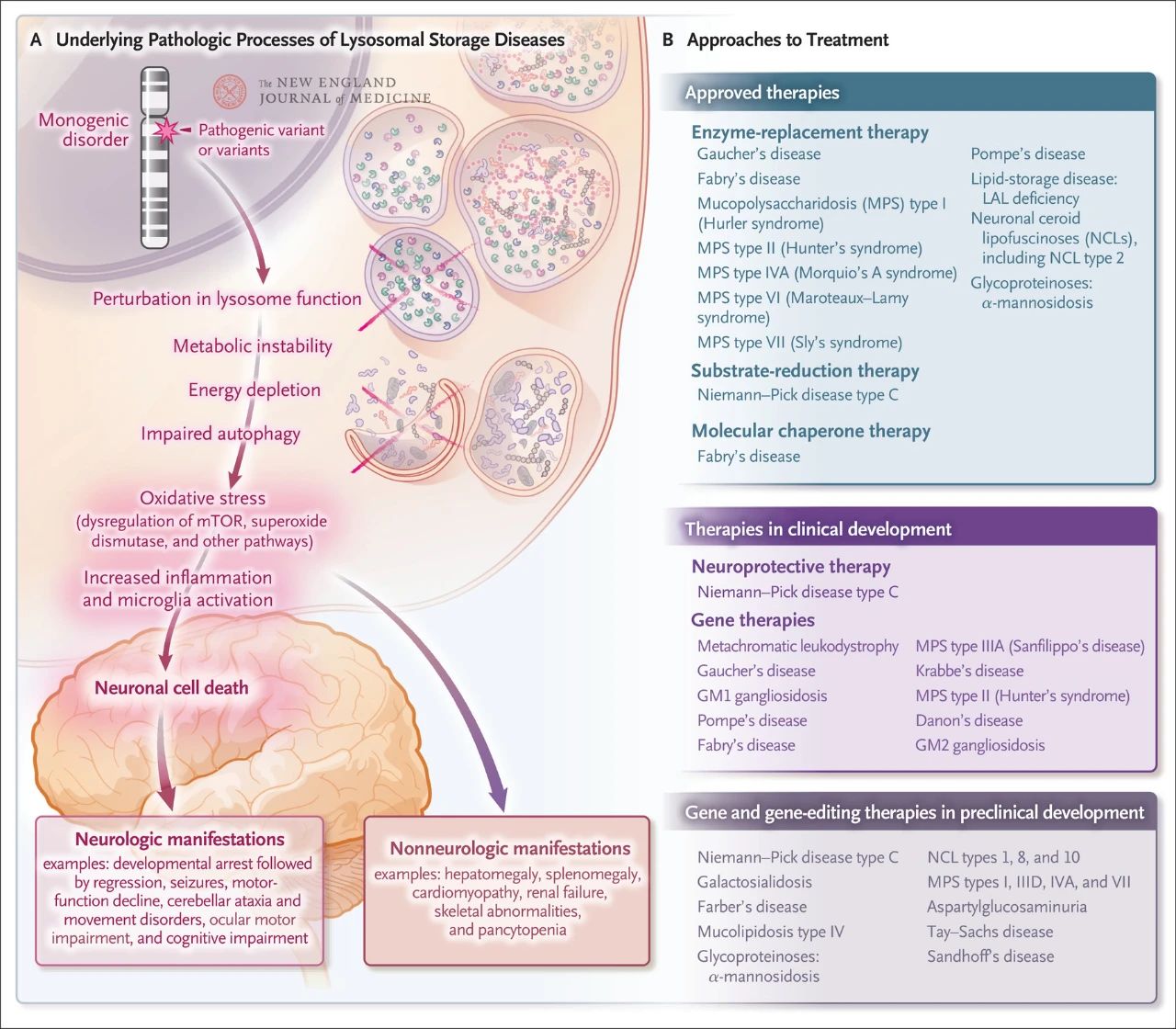
Bien que relativement rare, l'incidence globale de la surcharge lysosomale est d'environ 1 sur 5 000 naissances vivantes. De plus, sur les près de 70 maladies de surcharge lysosomale connues, 70 % touchent le système nerveux central. Ces maladies monogéniques provoquent un dysfonctionnement lysosomal, entraînant une instabilité métabolique, une dysrégulation de la protéine cible de la rapamycine chez les mammifères (mTOR, qui inhibe normalement l'inflammation), une altération de l'autophagie et la mort des cellules nerveuses. Plusieurs thérapies ciblant les mécanismes pathologiques sous-jacents de la maladie de surcharge lysosomale ont été approuvées ou sont en cours de développement, notamment l'enzymothérapie substitutive, la réduction du substrat, la thérapie par chaperons moléculaires, la thérapie génique, l'édition génique et la neuroprotection.
La maladie de Niemann-Pick de type C est une maladie lysosomale du transport du cholestérol causée par des mutations bialléliques du gène NPC1 (95 %) ou NPC2 (5 %). Les symptômes de la maladie de Niemann-Pick de type C incluent un déclin neurologique rapide et fatal pendant la petite enfance, tandis que les formes juvéniles tardives, juvéniles et adultes incluent une splénomégalie, une paralysie supranucléaire du regard, une ataxie cérébelleuse, une dysarticulation et une démence progressive.
Dans ce numéro de la revue, Bremova-Ertl et al. présentent les résultats d'un essai croisé en double aveugle, contrôlé par placebo. Cet essai utilisait un agent neuroprotecteur potentiel, l'analogue d'acide aminé N-acétyl-L-leucine (NALL), pour traiter la maladie de Niemann-Pick de type C. Ils ont recruté 60 patients symptomatiques, adolescents et adultes, et les résultats ont montré une amélioration significative du score total (critère d'évaluation principal) de l'échelle d'évaluation de l'ataxie.
Les essais cliniques sur la N-acétyl-DL-leucine (Tanganil), un racémique de NALL et de n-acétyl-D-leucine, semblent largement guidés par l'expérience : son mécanisme d'action n'a pas été clairement élucidé. La N-acétyl-dl-leucine est approuvée pour le traitement des vertiges aigus depuis les années 1950 ; des modèles animaux suggèrent que le médicament agit en rééquilibrant la surpolarisation et la dépolarisation des neurones vestibulaires médians. Par la suite, Strupp et al. ont rapporté les résultats d'une étude à court terme au cours de laquelle ils ont observé une amélioration des symptômes chez 13 patients atteints d'ataxie cérébelleuse dégénérative d'étiologies diverses, des résultats qui ont ravivé l'intérêt pour un nouvel examen du médicament.
Le mécanisme par lequel la n-acétyl-DL-leucine améliore la fonction nerveuse n'est pas encore élucidé, mais les résultats obtenus dans deux modèles murins, l'un de la maladie de Niemann-Pick de type C et l'autre de la variante O du syndrome de surcharge ganglioside à GM2 (maladie de Sandhoff), une autre maladie lysosomale neurodégénérative, ont incité l'attention à se tourner vers la NALL. Plus précisément, la survie des souris Npc1-/- traitées par la n-acétyl-DL-leucine ou la NALL (énantiomères L) s'est améliorée, tandis que celle des souris traitées par la n-acétyl-D-leucine (énantiomères D) ne s'est pas améliorée, suggérant que la NALL est la forme active du médicament. Dans une étude similaire sur la variante O du syndrome de surcharge ganglioside à GM2 (Hexb-/-), la n-acétyl-DL-leucine a entraîné une prolongation modeste mais significative de la durée de vie chez la souris.
Afin d'explorer le mécanisme d'action de la n-acétyl-DL-leucine, les chercheurs ont étudié la voie métabolique de la leucine en mesurant les métabolites dans les tissus cérébelleux des animaux mutants. Dans un modèle O variant de la maladie de stockage des gangliosides GM2, la n-acétyl-DL-leucine normalise le métabolisme du glucose et du glutamate, augmente l'autophagie et augmente les taux de superoxyde dismutase (un piégeur d'oxygène actif). Dans le modèle C de la maladie de Niemann-Pick, des modifications du métabolisme du glucose et des antioxydants ainsi qu'une amélioration du métabolisme énergétique mitochondrial ont été observées. Bien que la L-leucine soit un puissant activateur de mTOR, aucun changement n'a été observé dans le taux ou la phosphorylation de mTOR après traitement par la n-acétyl-DL-leucine ou ses énantiomères dans les deux modèles murins.
L'effet neuroprotecteur de la NALL a été observé dans un modèle murin de lésion cérébrale induite par un impact cortical. Ces effets comprennent une diminution des marqueurs neuro-inflammatoires, une réduction de la mort cellulaire corticale et une amélioration du flux autophagique. Après le traitement par NALL, les fonctions motrices et cognitives des souris lésées ont été restaurées et la taille de la lésion a diminué.
La réponse inflammatoire du système nerveux central est la caractéristique principale de la plupart des maladies lysosomales neurodégénératives. Si la neuroinflammation peut être réduite grâce au traitement de la NALL, les symptômes cliniques de nombreuses maladies lysosomales neurodégénératives, voire de toutes, pourraient être améliorés. Comme le montre cette étude, la NALL devrait également présenter des synergies avec d'autres traitements de la maladie lysosomale.
De nombreux troubles de surcharge lysosomale sont également associés à l'ataxie cérébelleuse. Selon une étude internationale menée auprès d'enfants et d'adultes atteints de troubles de surcharge des gangliosides GM2 (maladie de Tay-Sachs et maladie de Sandhoff), l'ataxie a été réduite et la coordination motrice fine améliorée après un traitement par NALL. Cependant, un vaste essai multicentrique, en double aveugle, randomisé et contrôlé par placebo a montré que la N-acétyl-DL-leucine n'était pas cliniquement efficace chez les patients atteints d'ataxie cérébelleuse mixte (héréditaire, non héréditaire et inexpliquée). Ce résultat suggère que l'efficacité ne pourrait être observée que dans le cadre d'essais portant sur des patients atteints d'ataxie cérébelleuse héréditaire et dont les mécanismes d'action associés ont été analysés. De plus, la NALL réduisant la neuroinflammation, susceptible d'entraîner des lésions cérébrales traumatiques, des essais de NALL pour le traitement des lésions cérébrales traumatiques pourraient être envisagés.
Date de publication : 02/03/2024